Cytotools: Günstiger Biotechwert mit Phantasie.
evtl. ist es schon bekannt, seit einiger Zeit hat CT auch einen neuen Presse Partner
Presse- und Investor Relationskontakt:
Instinctif Partners
Dr. Robert Mayer/Dorothea Schneider
Rindermarkt 5
80331 München
Tel.: +49-89-3090 5189 13
E-Mail: cytotools@instinctif.com
Die Meldung/Zusammenfassung der HV kam von der Gesellschaft. Beide Personen waren anwesend.
Soweit mir bekannt wurde auch die Hompage von Instinctif Partners erstellt.
Instinctif Partners ist ein Weltweit tätiges Unternehmen. CT hat sich hier keinen Wald- und Wiesenpartner zur Seite gestellt.
Denke CT ist auf einem guten Weg.
Ich war auch auf der HV, für mich klang das Statement von Dr. Freyberg nicht so eindeutig. Ein Verkauf von Dermatools schloss er nicht aus.
Gruß
eventuell kaufe ich bald wieder zu.
übrigens paion wird mir auch immer interessanter. schwere entscheidung irgendwie.
Hier mal zwei:
Es wird bald eine neu Nachricht kommen die uns alle freuen wird.
Wir können ja nicht sagen "hoppla, wir haben ja die Zulassung und was machen wir jetzt?"
Selbstverständlich arbeiten/planen wir den Verkauf und die Vermarktung schon heute.
Hat er so nicht wörtlich gesagt, aber vom Sinn her.
Die Vorstände selbst sind die Entwickler/Erfinder und wer verkauft schon sein Lebenswerk, außer er hat das entsprechende Alter oder ist bedürftig, was in beiden Fällen nicht gegeben ist. Das klare Ziel des Vorstandes und so wurde das auf der HV auch geäußert ist, das Maximum für DermaPro zu erwirtschaften. Das ist unter Berücksichtigung der "Mehrfachindikationen" sicherlich nicht über einen Verkauf zu erzielen.
Resultat: Die Option Verkauf steht meiner Meinung nach ganz hinten an.
Ich gehe davon aus, dass man in Kürze einen europäischen Partner vorstellen wird, der sich um die Vermarkung kümmern wird, vergleichbar mit Centaur in Indien.
Also macht euch nicht verrückt.....
mag sein, dass die vorstände bei einem superpreis für dermatools zu einem verkauf bereit sind, doch die filetstücke in der entwicklung werden sie bestimmt behalten. das marktreife produkt dermapro für das diabetische fußsyndrom, das die geringeren umsätze beisteuert, kann man in dieser hinsicht schon verkaufen, es sind ja bei cytopharma ebenso noch blockbusters im höheren milliardenbereich vorhanden.
diese leute wissen genau, was sie tun und ich glaube alle maßgebenden beteiligten bei der ag und den gmbh´s wollen in der forschung und entwicklung noch einige jahre tätig sein.
im gegensatz zu vielen anderen biotechs haben sie viele lukrative entwicklungen im köcher.
ein verkauf von dermatools, ohne die geplanten neuentwicklungen, hätte für cytotools einen entscheidenden vorteil, nämlich keine zeit zu verlieren, die kostenaufwändige vermarktung zu vermeiden und freie entwicklung für die indikationen zu haben, die ein mehrfaches dieser umsätze bringen.
mir wäre eine cytoools mit der kompletten dermatools natürlich lieber, doch ein beinbruch ist es nicht, wenn der diabetische fuß und ein wenig anderes verkauft wird.
nochmal besten dank an alle von ariva und wallstreet online für die hv-berichte, ohne euch hätten wir keine möglichkeit darüber etwas zu erfahren, die allgemeine presse schweigt.
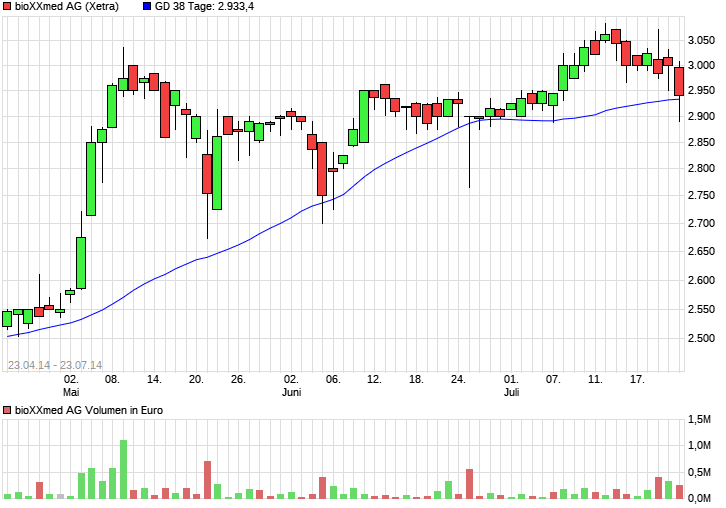
der kurs will nicht über 60, doch irgendwann in den nächsten wochen tut er es.
Das Produkt kann noch so gut sein, wenn der Vertrieb nicht läuft kommt auch kein Umsatz.
Wenn ich das auf der HV zwischen den Zeilen richtig gelesen habe, könnte es sich um diese freudige Neuigkeit handeln.
Die neue Presseagentur hat auch den Auftrag Produkt und Firma auf dem Weltmarkt einen gewissen Bekanntheitsgrad/Aufmerksamkeit zu generieren.
Hatte auch den Eindruck Dr. Freyberg war und ist sehr stolz auf sein Unternehmen. Ist ja auch gut für uns, denn irgendwie ist es ja doch eine Firma die noch wie ein Familienunternehmen geführt wird.
da steigt wohl einer dick ein hier, wenn man mal hochrechnet
habe auch so verstanden dass der Vertrieb auf keinen Fall von CT direkt betrieben wird. Wie auch mit fünf Leuten?

07:33 24.07.14
BB BIOTECH AG / BB Biotech verzeichnet weitere Erfolgsmeldung im Portfolio . Verarbeitet und übermittelt durch NASDAQ OMX Corporate Solutions. Für den Inhalt der Mitteilung ist der Emittent verantwortlich. Source: Globenewswire
Portfoliogesellschaft Puma Biotechnology mit Durchbruch bei HER2-positivem Brustkrebs
Das Medikament Neratinib der US-Firma Puma Biotechnology hat in einer Phase-III-Studie überzeugt und sein Potenzial als Blockbuster-Medikament bestätigt. Die Meldung hat dem Börsenkurs des Unternehmens massiven Auftrieb gegeben und fast zu einer Vervierfachung der Kapitalisierung geführt. BB Biotech hält per 22. Juli 2014 insgesamt 576'991 Titel, was einem Anteil von 1.4% des Inneren Wertes der Beteiligungsgesellschaft entspricht.
bei puma biotechnology handel es sich um ein unternehmen mit aktuell 6,37 mrd. dollar mcap.
PS: Hoffe für dich, dass du investiert bist/warst
puma kenne ich erst seit gestern, als ich die bb biotech-meldung las. leider.
der beitrag von comedy zur hv: 2. quartal 2015 fertigstellung phase II/III offenes bein
europa
fertigstellung phase III diabet. fuß europa
erfolgt offenbar früher, als ich dachte. in den nächsten 9 monaten wird es viele fundamentale, kurstreibende meldungen zu cytotools geben und das fast egal, wie der gesamtmarkt tendiert.
geht´s noch besser?
immerhin warten auf cytotools 100 mio. kunden mit offenen wunden weltweit. neuerkrankungen jährlich von 10 mio. menschen geben hier auch das langfristige umsatzpotential (vielleicht sind es auch 200 mio und 8 mio?).
CytoTools AG: Klinische Entwicklung des Wundheilungspräparates DermaPro(R) in Europa läuft planmäßig und eine erste Analyse gibt Hinweise, dass sich die Daten aus der Phase IIb bestätigen
10:50 25.07.14
DGAP-News: CytoTools AG / Schlagwort(e): Sonstiges
CytoTools AG: Klinische Entwicklung des Wundheilungspräparates
DermaPro(R) in Europa läuft planmäßig und eine erste Analyse gibt
Hinweise, dass sich die Daten aus der Phase IIb bestätigen
25.07.2014 / 10:48
--------------------------------------------------
Klinische Entwicklung des Wundheilungspräparates DermaPro(R) in Europa
läuft planmäßig und eine erste Analyse gibt Hinweise, dass sich die Daten
aus der Phase IIb bestätigen
- "Diabetischer Fuß": Über 200 Patienten für die laufende Phase III Prüfung
in der Indikation in die Studie aufgenommen
- Unabhängiges "Data Safety and Monitoring Board" (DSMB) empfiehlt, die
Phase III Studie wie geplant fortzuführen und gibt damit den klaren
Hinweis, dass sich die guten Ergebnisse der Phase IIb bestätigen
- Experten des Bundesinstituts für Arzneimittel und Medizinprodukte (BfArM)
bestätigen in einem wissenschaftlichen Beratungsgespräch grundsätzlich den
Entwicklungsplan der DermaPro(R) Wundheilungslösung
- Ulcus Cruris (offenes Bein): Phase II/III Studie in der Indikation hat
mit dem Screening und der Rekrutierung von Patienten begonnen
Darmstadt, 25. Juli 2014 - Die DermaTools Biotech GmbH, eine
Tochtergesellschaft der CytoTools AG, ist mit dem zeitgerechten Verlauf
ihrer in 2013 begonnenen Phase III Studie in der Indikation "diabetischer
Fuß" sehr zufrieden. Mehr als 200 Patienten wurden bereits in die
therapeutische Phase der Studie in Deutschland und dem europäischen Ausland
aufgenommen. Eine erste verblindete Interimsanalyse anhand der
ausgewerteten Daten der ersten 80 Patienten, die die Studie beendet haben,
wurde am 23.07.2014 durch ein unabhängiges DSMB vorgenommen. Das DSMB
empfiehlt die unveränderte Fortführung der Studie. Dies ist als klarer
Hinweis zu werten, dass sich die guten Ergebnisse der europäischen Phase
IIb Studie bestätigen. Eine unverblindete Interim-Analyse wird nach
Abschluss der ersten 160 Patienten im 4. Quartal erwartet, bei der dann
schon konkrete Hinweise über die voraussichtliche Wirksamkeit in dieser
Zulassungsstudie von DermaPro(R) vorgestellt werden können.
In einem Treffen mit Experten des BfArM im Juni 2014 wurde der DermaPro(R)
Entwicklungsplan zur Erlangung der Zulassung grundsätzlich bestätigt. Es
wurden weder Vorgaben gemacht noch Einwände erhoben, die die für 2015
geplante Einreichung zur Zulassungsgenehmigung in Europa verzögern könnten.
Ulcus Cruris (offenes Bein)
Parallel hierzu hat die europäische klinische Phase II/III in der
Indikation Ulcus Cruris begonnen und die ersten Patienten werden
rekrutiert. Auch diese Studie befindet sich im Plan und wird bei der
Zulassungseinreichung als zweite zulassungsrelevante Studie eingereicht
werden können. Damit kann eine Zulassung gleich für zwei Indikationen in
Europa erreicht werden.
"Insgesamt sind wir mit dem Verlauf unseres klinischen
Entwicklungsprogramms derzeit sehr zufrieden", erläutert Dr. Markus
Weissbach, Chief Medical Officer von CytoTools AG. "Die klinische
Entwicklung von Arzneimitteln birgt manchmal Überraschungen, von denen wir
bisher verschont geblieben sind. Dies ist nicht nur auf das nach wie vor
hervorragende Sicherheitsprofil von DermaPro(R) zurückzuführen, sondern
auch auf das zunehmende Vertrauen unserer Prüfärzte in die sehr gute
Wirksamkeit unserer Substanz und ihre unkomplizierte Anwendung", so
Weissbach in seiner Stellungnahme.
Diese Mitteilung enthält bestimmte in die Zukunft gerichtete Aussagen.
Diese spiegeln die Meinung von CytoTools zum Datum dieser Mitteilung wider.
Die von CytoTools tatsächlich erzielten Ergebnisse können von den
Feststellungen in den zukunftsbezogenen Aussagen erheblich abweichen.
CytoTools ist nicht verpflichtet, in die Zukunft gerichtete Aussagen zu
aktualisieren.
Über CytoTools:
Die CytoTools AG ist ein deutsches Biotech-Unternehmen, das Ergebnisse aus
der zellbiologischen Grundlagenforschung zu Zellwachstum und programmiertem
Zelltod in neuartige Therapieformen zur ursächlichen Krankheitsbehandlung
und Heilung umsetzt. Die Firma hat eine stabile und diversifizierte
Produktpipeline von ursächlich wirksamen biologischen und chemischen
Wirkstoffen aufgebaut. Diese zeigen das Potenzial für neue
Behandlungsmöglichkeiten in der Dermatologie, Kardiologie und Angiologie,
Urologie und Onkologie. CytoTools ist als Technologieholding - und
Beteiligungsunternehmen strukturiert und hält als solches Beteiligungen an
den Tochterfirmen DermaTools Biotech GmbH (57%) und CytoPharma GmbH (42%).
Kontakt:
CytoTools AG
Dr. Mark Andre Freyberg
Klappacher Str. 126
64285 Darmstadt
Tel.: +49-6151-95158-12
Fax: +49-6151-95158-13
E-Mail: freyberg@cytotools.de
Presse- und Investor Relationskontakt:
Instinctif Partners
Dr. Robert Mayer/Dorothea Schneider
Rindermarkt 5
80331 München
Tel.: +49-89-3090 5189 13
E-Mail: cytotools@instinctif.com
Ende der Corporate News
--------------------------------------------------
25.07.2014 Veröffentlichung einer Corporate News/Finanznachricht,
übermittelt durch die DGAP - ein Unternehmen der EQS Group AG.
Für den Inhalt der Mitteilung ist der Emittent / Herausgeber
verantwortlich.
Die DGAP Distributionsservices umfassen gesetzliche Meldepflichten,
Corporate News/Finanznachrichten und Pressemitteilungen.
Medienarchiv unter http://www.dgap-medientreff.de und
http://www.dgap.de
die umsätze und kurse sind am steigen aufgrund der meldung
Cyto wird täglich mehr wert (nicht nur kursmäßig sondern vor allem auch kontinuierlich strategisch) und wir dürfen daran teilhaben.
Da können doch auch wir schon mal langsam sehr
zufrieden in ein schönes Wochenende starten. :)
Bis auf weiteres.
Ich gehe mal davon aus, dass das die Nachricht war, die uns Dr. Freyberg auf der HV am 22.7. voller Stolz angekündigt hat, über die wir uns alle freuen würden...... Wenn ich mir den heutigen Kursverlauf anschaue, bin ich schon ziemlich gefrustet. Das Volumen steigt doch der Kurs nicht wirklich? Jetzt kommen bestimmt einige und sagen: "... ist halt schon alles eingepreist..." usw. Ich hab mir das wirklich anders vorgestellt, wenn ich mir anschaue, was gestern bei Puma abging? +400% nur weil die eine Phase III Studie erfolgreich abgeschlossen haben? Hatten wir das nicht auch schon?
Gehe jetzt gefrustet ins Wochenende ;-(
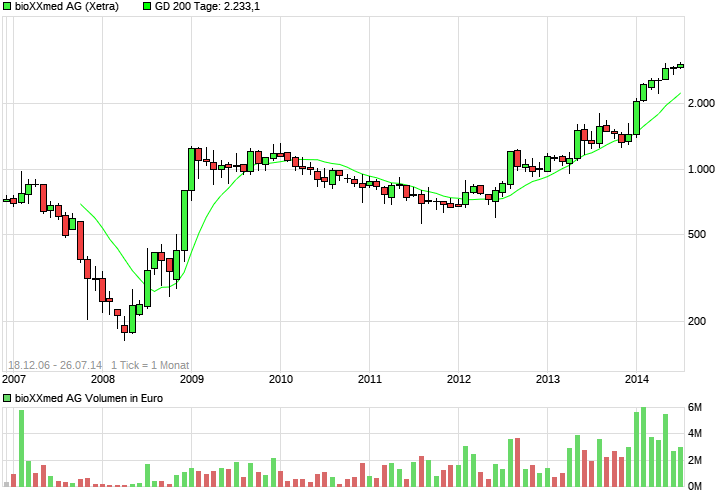
der monatschart seit 2007 sieht für dieses jahr doch sehr positiv aus. der deckel wird nicht mehr lange halten, im kurs ist eindeutig zu wenig eingepreist. ich versuche seit längerer zeit zu verstehen warum der kurs so undefinierber reagiert.
die fakten hierzu sind von der medizinischen seite:
- eine story mit mehreren potentiellen blockbustern, derma und cardio
- keine nebenwirkungen und völlig problemlose lagerung von dermapro
- niedrige herstellungskosten von dermapro
- hohes interesse auf der fachärzteseite für dermapro
- zunehmende demografische neuerkrankungen
- größtenteils sehr eingeschränkte lebensqualität der erkrankten
- heilungsquote von dermapro um 90%
- völlig unbefriedigende medizinische indikationen der bestehenden konkurrenzfirmen
teilweise viel zu hohe behandlungskosten
- hervorragendes fachpersonal in allen drei firmen
- wiederholte verzögerungen in klinischen phasen
- dez. 2013 zulassungsantrag bei der indischen behörden
- geplanter zulassungsantrag für diabetischen fuß brd/europa und ulcus curius brd/europa
im 3. quartal 2015
- jüngste positive feedbacks vom bundesinstitut für arzneimittel und medizinprodukte und einer unabhängigen expertengruppe für patientensicherheit und therapieerfolg zur indikation von dermapro
die fakten zur aktie selbst
- freiverkehr
- zwei destinated sponsors, die nichts öffentlich publizieren
- ein sehr hohes institutionelles interesse
- eine hohe beteiligungsquote der direkten insider (ankerinvestoren u. gmbh-gesellschafter)
- cytotools hat viele anfragen für eine außerbörsliche beteiligung
- die eurams-meldung sieht für mich nach einer manipulierten meldung aus
- eine hochinteressante fundamentale story
- die umsätze steigen seit 2014 stärker an
- ein längerer gedeckelter kursverlauf
- kein nennenswertes öffentliches bzw. analysteninteresse
- kursrückgänge, ein paar tage nach den pressemeldungen
das einzige, was sich für mich daraus ergibt ist ein hohes institutionelles an der aktie, nur gibt es nicht genügend material am markt, vor allem nicht zu kursen unter oder um 60 euro.
diese marktteilnehmer sind offenbar nicht oder noch nicht bereit wesentlich mehr zu bezahlen.
Original-Research: CytoTools AG (von GBC AG): Kaufen
09:31 28.07.14
Original-Research: CytoTools AG - von GBC AG
Einstufung von GBC AG zu CytoTools AG
Unternehmen: CytoTools AG
ISIN: DE000A0KFRJ1
Anlass der Studie: Research Comment
Empfehlung: Kaufen
Kursziel: 73,30 Euro
Kursziel auf Sicht von: Ende GJ 2015
Letzte Ratingänderung:
Analyst: Cosmin Filker, Manuel Hölzle
Planmäßiger Verlauf der finalen Studienphase III in Europa - Ausweitung auf
den Indikationsbereich 'Ulcus Cruris' birgt weitere Potenziale
Gemäß aktueller Unternehmensmeldung schreitet die europäische klinische
Studienphase III für den Indikationsbereich 'Diabetischer Fuß' planmäßig
voran. Seit April 2014 konnten für die klinische Studienphase weitere 60
Patienten in Deutschland und dem europäischen Ausland aufgenommen werden,
so dass aktuell insgesamt 200 Patienten einbezogen sind. Im Rahmen der
finalen und für die gesamteuropäische Zulassung ausschlaggebenden
klinischen Studienphase III muss die Wirksamkeit von DermaPro(R) an
insgesamt 350 Teilnehmern erprobt werden.
Darüber hinaus liefern die ersten Vorabergebnisse konkrete Hinweise zur
Wirksamkeit des Wundheilungspräparates DermaPro(R). Gemäß
Unternehmensmitteilung hat sich ein unabhängiges Gremium, nach der Sichtung
der ersten ausgewerteten Daten, für die Fortführung der Studie
ausgesprochen, was als ein positives Signal hinsichtlich der Wirksamkeit
und der damit verbundenen Zulassung des Cytotools-Produktes zu verstehen
ist. Grundsätzlich wurde der Zulassungszeitplan nach Rücksprache mit BfArM
bestätigt und folglich bestätigen wir auch unseren produktions- und
umsatzbezogenen Zeitplan.
Die ersten Vermarktungserlöse in Europa dürften demnach im Geschäftsjahr
2016 erzielt werden. Zusätzlich zum Indikationsgebiet 'diabetischer Fuß'
ist auch eine Zulassung für den Indikationsbereich 'Ulcus Cruris' geplant.
Mit der Rekrutierung der ersten Patienten hat bereits die kombinierte
klinische Phase II/III in Europa begonnen. Sollten die erwartet guten
Resultate auch beim Ulcus Cruris in der Studienphase II bestätigt werden,
besteht die Möglichkeit einer gleichzeitigen Abdeckung der Studienphase
III. Damit ist mit einem deutlich verkürzten Zeitaufwand für die klinische
Zulassung bei Ulcus Cruris zu rechnen.
Angesichts der planmäßigen Studienverlaufs behalten wir unsere bisherigen
Schätzungen bei (siehe Researchstudie vom 08.07.14) und bestätigen das
Kursziel von 73,30 EUR und das Rating KAUFEN.
Die vollständige Analyse können Sie hier downloaden:
http://www.more-ir.de/d/12395.pdf
Kontakt für Rückfragen
Jörg Grunwald
Vorstand
GBC AG
Halderstraße 27
86150 Augsburg
0821 / 241133 0
research@gbc-ag.de
-------------------übermittelt durch die EQS Group AG.-------------------
Für den Inhalt der Mitteilung bzw. Research ist alleine der Herausgeber bzw.
Ersteller der Studie verantwortlich. Diese Meldung ist keine Anlageberatung
oder Aufforderung zum Abschluss bestimmter Börsengeschäfte.
Hinweis: ARIVA.DE veröffentlicht in dieser Rubrik Analysen, Kolumnen und Nachrichten aus verschiedenen Quellen. Verantwortlich für den Inhalt ist allein der jeweilige Autor.