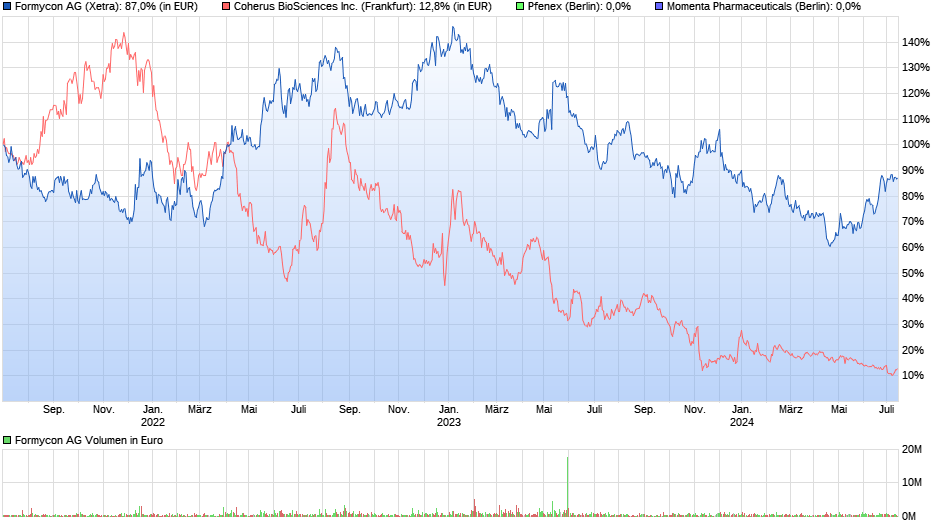
Pfenex Formycon Coherus Momenta Biosimilarwerte
Novartis has been losing ground in the age-related macular degeneration (AMD) market, but a pair of positive phase 3 trials for new drug brolucizumab (aka RTH258) suggests a comeback could be on the cards.
AMD affects up to 25 million people worldwide and is the leading cause of early blindness in the industrialized world, and for some years Novartis' VEGF inhibitor Lucentis (ranibizumab) was the leading treatment for the wet or 'neovascular' form of the disease.
Latterly however the drugmaker, along with partner Roche, has been in a toe-to-toe battle with Bayer and Regeneron, whose rival VEGF/PIGF inhibitor Eylea (aflibercept) has been in the ascendency despite Lucentis' first-to-market advantage.
https://seekingalpha.com/news/...834-hits-bump-road-early-stage-study
Coherus down 13% on Amgen launch of single-dose cartridge version of Enbrel
Nov. 17, 2017 3:36 PM ET|About: Coherus BioSciences (CHRS)|By: Douglas W. House, SA News Editor
Coherus BioSciences (CHRS -13.2%) slumps on almost double normal volume in apparent response to Amgen's launch of ENBREL Mini, a single-dose prefilled cartridge designed for self-administration via an autoinjector.
One of Coherus' late-stage product candidates, CHS-0214, is a biosimilar to Enbrel (etanercept) but it will not be offered, at least initially, in a like format.
Previously: Amgen launches Enbrel in single-dose cartridge format for autoinjector (Nov. 17)
Novartis peilt die Zulassung eines neuen Augen-Medikaments an. Das Problem: Das Unternehmen konkurrenziert damit Lucentis, das Produkt, das es für von Roche ausserhalb der USA vertreibt.
https://seekingalpha.com/news/...e-mid-stage-studies-shares-1-percent
WERBUNG
von FYB202 beteiligt * Entwicklung des Biosimilar-Kandidaten bis zur Zulassung geplant
Das Biosimilar-Unternehmen Formycon AG (ISIN: DE000A1EWVY8/ WKN: A1EWVY) und die Aristo Pharma GmbH, ein pharmazeutisches Unternehmen mit Sitz in Berlin, haben ein gemeinsames Unternehmen zur weiteren Entwicklung von FYB202, Formycons Biosimilar-Kandidat für Stelara®* (Ustekinumab), gegründet. An der Gesellschaft, die den Namen FYB202 GmbH & Co. KG trägt, sind Formycon mit 24,9 Prozent und Aristo Pharma mit 75,1 Prozent beteiligt. Zwischen den Partnern wurde vereinbart, dass nach einer Pilotphase die weiteren Entwicklungskosten sowie die bisherigen Projektinvestitionen der Beteiligungsquote entsprechend getragen werden sollen. Analog sollen beide Unternehmen entsprechend ihrer Quote an den zu erwartenden Lizenzerträgen partizipieren.
Ziel des Joint Ventures ist es, den Biosimilar-Kandidaten bis zur Zulassung zu entwickeln, wobei Formycon Teile der weiteren Entwicklungsarbeit übernehmen wird.
Bei Stelara® (Ustekinumab) handelt es sich um einen humanen monoklonalen Antikörper, der gegen die Zytokine Interleukin-12 und Interleukin-23 gerichtet ist und zur Behandlung verschiedener schwerwiegender inflammatorischer Erkrankungen wie mittelschwerer bis schwerer Psoriasis (Schuppenflechte) eingesetzt wird. Im Jahr 2016 erfolgte eine Indikationserweiterung für die Behandlung von Morbus Crohn, einer chronisch-entzündlichen Darmerkrankung.
Momenta Pharmaceuticals Inc and Mylan NV plan to begin a pivotal clinical trial of a biosimilar to Regeneron Pharmaceuticals Inc’s blockbuster eye drug Eylea in the first half of this year, the two companies said on Wednesday.
If successful, it would likely mark the first competition from a cheaper biosimilar of Eylea, although Regeneron says it has U.S. patent protection on the treatment until 2023.
Germany’s Formycon AG is far along in testing a biosimilar to Eylea rival Lucentis from Roche. It lists an Eylea biosimilar at the preclinical stage on its pipeline chart, putting it behind the Momenta/Mylan candidate.
Our preclinical-stage pipeline consists of CHS-3351, a ranibizumab (Lucentis) biosimilar product candidate, and CHS-2020, an aflibercept (Eylea) biosimilar candidate. We have completed cell-line development for our CHS-3351 candidate and clarified our manufacturing, clinical and regulatory path with the FDA. We expect to begin clinical trials for CHS-3351 in 2018
Formycon ist der einzige Entwickler, der sein Lucentis Biosimilar in Phase 3 hat und einige Adressen munkeln, dass hier bald Ergebnisse anliegen. Ich möchte aber betonen, dass es sich hierbei um Gerüchte handelt. Coherus wollte dieses Jahr in die klinische Entwicklung und Pfenex ist weiterhin bemüht einen neuen Partner zu finden.
Damit gibt es in dieser frühen Phase einen Wettbewerber zu Formycons FYB 202, dem Stelara Biotechsimilar.
Es werden vorklinische Daten von NeuClone präsentiert.